食道・胃・十二指腸ペプチドワクチン療法
~臨床第II相試験で食道がん術後の生存率を約2倍に改善することに成功!~
近畿大学病院上部消化管外科(研究代表者:安田卓司)と東京大学医科学研究所の中村祐輔先生(当時)のチームは、共同研究として食道がんに対するがんペプチドワクチンの臨床試験に約10年間取り組んできましたが、漸く昨年最終解析が終了し、世界で初めてペプチドワクチンのがん治療における有効性を証明することに成功しました。この結果は、2020年8月29日付で外科領域のトップジャーナルである「Annals of Surgery」(インパクトファクター:10.13)にオンライン掲載されました。
今、注目される免疫療法
ノーベル賞を受賞された本庶佑先生のチームが免疫系にブレーキをかける「PD-1」という受容体を発見して以来、がんに対する免疫療法に注目が集まっています。これまでのがん治療、特に消化器がんに関しては、手術、抗がん剤(化学療法)、放射線治療が3本柱で、そのいずれもがからだには有害な、身を削る治療でありました。それに対して4番目の柱として加わった免疫療法は、自己のもつがん免疫を活性化して全身に潜んでいるがん細胞を根絶させるという、人間のからだがもつ本来の力を強化するがん治療です。
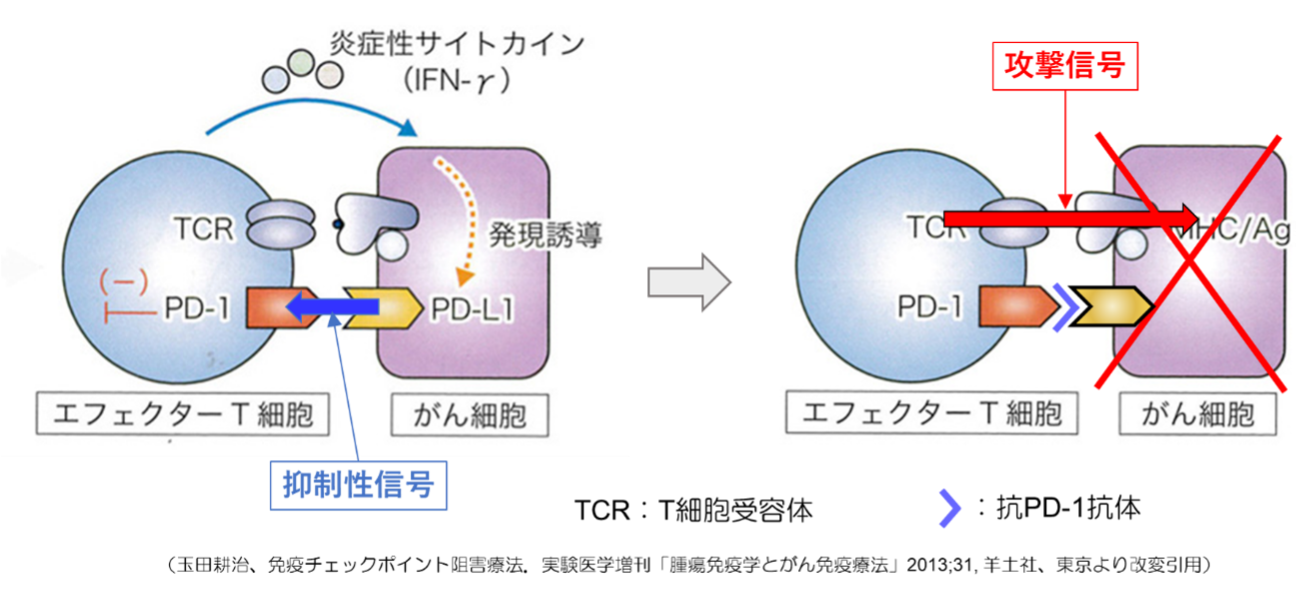
ここで簡単に現在注目されている免疫療法について説明しておきます。今の免疫療法は以前のものとは全く異なります。外的に対する免疫には、アレルゲンに対する免疫からウイルスや細菌に対する免疫、がんに対する免疫まで様々です。以前はリンパ球を取り出し活性化して体内に戻す治療などが行われましたが、これはがんに対する免疫を活性化しているとは限らず、非特異的免疫療法といいます。それに対して現在行われているのは、がん細胞を攻撃する細胞だけを活性化してがん細胞の根絶を図るという特異的免疫療法です。がん細胞を攻撃する細胞は、細胞傷害性T細胞といいます。この細胞ががん細胞を見つけ出して攻撃するのですが、免疫の暴走を防ぐために車と同様にブレーキの役目を果たす「PD-1」受容体を細胞表面にもっています。ところが、がん細胞は免疫の攻撃を受けると細胞表面に「PD-L1」というPD-1受容体と特異的に結合する細胞分子を発現させ、PD-L1とPD-1の結合を介して抑制性信号を細胞傷害性T細胞に送ります。その結果、細胞傷害性T細胞は無力化し、がん細胞は免疫の攻撃を回避して生き残って増殖していきます。一方、免疫チェックポイント阻害薬というのは、このPD-1とPD-L1の結合を阻害する「抗PD-1抗体」という抗体薬です。これががん細胞からの抑制性信号をブロックすることで細胞傷害性T細胞は再活性化し、再びがん細胞を攻撃して根絶を図るというのが今の免疫療法です(図1)。例えでいうと、がん細胞が利用する「PD-1/PD-L1結合」は自身を守る"盾"であり、細胞傷害性T細胞はがん細胞を攻撃する"鉾"にあたります。免疫チェックポイント阻害薬はがん細胞の守りの"盾"を取り除く治療です。しかし、いくら相手が無防備であっても肝心の"鉾"がない、あるいは弱ければがん細胞を排除することはできません。この"鉾"にあたる細胞傷害性T細胞を強化・増強するのがペプチドワクチン療法です。つまり、免疫チェックポイント阻害薬とはがん細胞の防御機構を無力化させる治療で、ペプチドワクチンとはがん細胞に対する攻撃を強化する治療です。
図1 がん細胞による免疫逃避機構と抗PD-1抗体による免疫の活性化機構
ペプチドワクチン療法とは
からだの中に異物であるがん細胞が生じると免疫はそれを排除します。しかし、がん細胞は少しずつ変化しながら生き残りを図り、免疫は徐々にがん細胞と正常細胞の区別がつきにくくなっていきます。例えでいうと、犯人が一般社会の中に溶け込んで一般人と判別つかなくなっている状況です。でも、がん細胞は正常細胞とは異なる特徴を細胞表面にペプチドとしてもっています。そのがん細胞特異的なペプチドの情報をワクチンとして免疫に情報提供することでその情報をもつ細胞はがん細胞であることを免疫に再認識させ、そのがん細胞を特異的に攻撃する細胞傷害性T細胞を大量に産生して全身に送り出すことでがんの根絶を図るというのがペプチドワクチン療法です。つまり、指名手配犯の顔写真をからだの警察である免疫に提供し、警察はその顔写真をもった警察官を全国に派遣して犯人を捜して捕まえるという治療です。
今回の食道がんに対するペプチドワクチン第II相臨床試験の研究成果の概要
食道がんは、進行が極めて早く、早期からかつ広範囲に転移を有するため、治癒切除し得ても多くが再発をきたす極めて予後不良の悪性腫瘍です。そのため、手術に加えて術後化学療法の追加が検討され、近年は術後よりも術前の方が有効であるということから術前に化学療法または化学放射線療法を追加して再発予防および切除率の向上を図っているところです。しかし、これらの治療の組み合わせにもかかわらず切除標本の検索でリンパ節にがんの転移が遺残している症例は依然予後は不良です。つまり、微小ながん細胞が全身にまだ残っているということで追加治療が必要と考えられますが、術前治療後に治癒切除された食道がん症例に対する術後の標準治療は未だ確立されていません。侵襲的な治療を続けた後の臓器機能の低下と潜在的な微少がん細胞が対象であることを考えると、免疫を強化し、免疫監視機構により微少がん細胞を見つけ出して特異的に攻撃するペプチドワクチン療法は良い適応であり、かつ効果が期待されると考えて本臨床試験を計画しました。
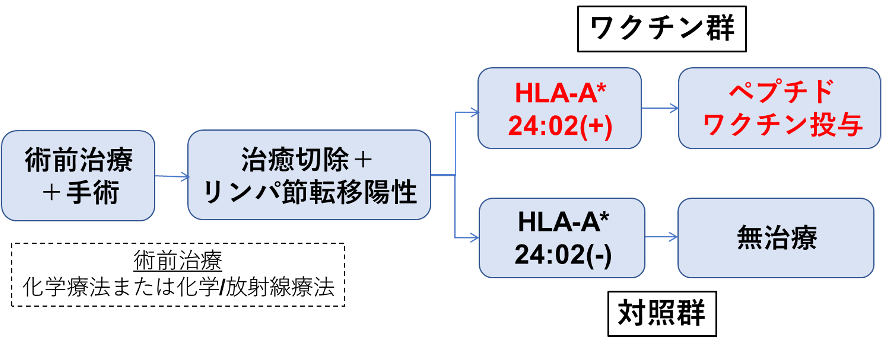
使用したペプチドワクチンは、中村先生のグループが世界で初めて発見した食道扁平上皮がん細胞(日本人の食道がんの9割以上を占める)の細胞表面に特異的に発現している3種類の抗原ペプチド(URLC-10、KOC-1、CDCA1)です。この3種類の抗原ペプチドをワクチンとして術後に投与しました。最初の10回は毎週、次の10回は隔週と合計20回皮下に投与をしました。ただ、投与した抗原ペプチドを情報として免疫が受け取るにはヒト白血球抗原(HLA)という分子が必要ですが、その中でも今回使用したペプチドの情報を強力に認識するには日本人の約6割が有しているHLA-A-2402というタイプであることが必要でした。そこで図2に示すように、術前治療後に治癒切除されるも病理学的にリンパ節転移が陽性であった食道扁平上皮がん症例をHLAのタイプで2群に分けて、HLA-A2402を有する患者にはワクチン治療を追加し、それ以外の患者は従来通り無治療で経過観察するというデザインで比較試験を行いました。最終的にワクチン群:33例、対照群:30例が登録されました。
図2 試験デザイン
ペプチドワクチンの術後再発予防効果
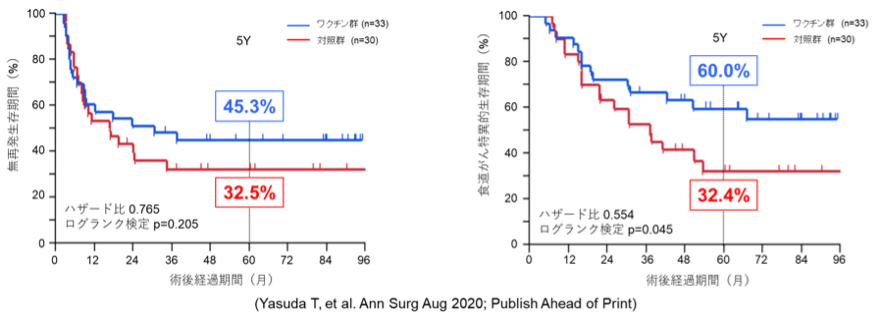
5年無再発生存率を比較すると、対照群の32.5%に対してワクチン群は45.3%と良好ではありましたが、その再発予防効果は統計学的に有意であるとはいえませんでした。ただ、食道がんによる死亡に着目して検討した5年食道がん特異的生存率は対照群の32.4%に対してワクチン群は60.0%と約2倍にその成績は改善されており、統計学的にも有意にペプチドワクチンによる予後改善効果が証明されました。
図3 ワクチンの予後改善効果
ペプチドワクチンが有効な症例の特徴
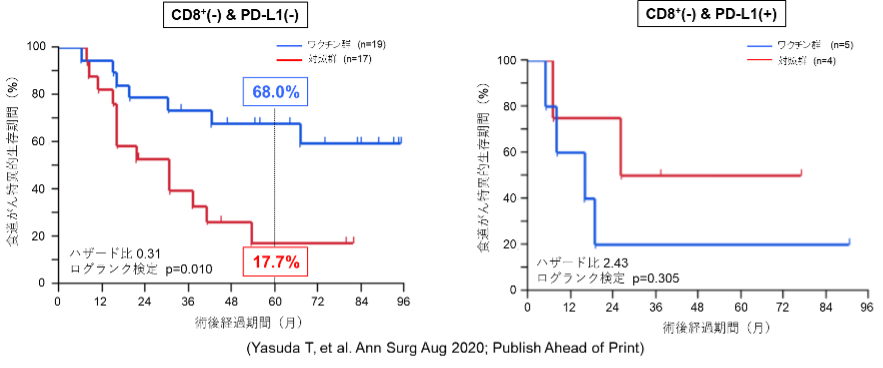
切除標本を用い、腫瘍内に入り込んだ細胞傷害性T細胞(CTL)の有無とがん細胞の表面におけるPD-L1の発現の有無で腫瘍の微少環境を評価し、その腫瘍環境と治療効果との関連を検討しました。その結果、全体の約6割を占めるCTL(-)/PD-L1(-)の腫瘍、つまり細胞傷害性T細胞も腫瘍内に認めず、がん細胞もPD-L1を発現していない腫瘍では、がん細胞は細胞傷害性T細胞を無力化することはできず、ワクチンで増強された細胞傷害性T細胞の効果で遺残する微小がん細胞は多くの症例で根絶され得ることが示されました。5年食道がん特異的生存率で対照群が僅か17.7%であるのに対してワクチン群は68.0%と約4倍にその成績が向上しているのは、ペプチドワクチンの強力な微小がん細胞の制御による再発予防効果と考えられました。一方、全体の約15%を占めるCTL(-)/PD-L1(+)の腫瘍においてはがん細胞表面のPD-L1が細胞傷害性T細胞表面のPD-1と結合して抑制性信号を送るため、数的に細胞傷害性T細胞は増幅されていたとしてもがん細胞を攻撃することができず、全くワクチンの効果は認められませんでした。しかし、このタイプの腫瘍に対しては免疫チェックポイント阻害剤を併用してPD-L1を介した抑制性信号をブロックすることで前者と同様の予後改善効果が得られると期待されます。
図4 腫瘍微小環境別にみたペプチドワクチンの効果
ペプチドワクチンの将来展望
本臨床試験の中間解析における有用性の結果を受けて、2015年からペプチドワクチンの治療薬としての保険承認を目指した企業主導の第III相臨床試験が行われ、2018年に登録が終了しました。本試験においては、近畿大学病院上部消化管外科の安田が治験責任医師を務め、全国の55施設から276例の登録を頂き、2021年に再発予防効果について解析を行う予定です。未だ世界的にみてもワクチン療法としては前立腺がんにおいてがんの情報を読み取る樹状細胞(じゅじょうさいぼう)を用いた治療がアメリカや欧州で治療薬として承認されているのみです。まだ、ペプチドワクチンとしての成功例はなく、第II相臨床試験においても我々の研究と同様の結果が証明され、日本発のペプチドワクチン治療薬が世界で初めて保険承認されることを期待しています。
ペプチドワクチンの有効性以外における第II相臨床試験の意義と重要性
- 基礎研究で発見された研究成果を医師主導第II相臨床試験においてその有用性を明らかにし、それを企業主導の臨床試験へと発展させて治療薬としての保険承認を目指すという創薬のあるべきモデルケースと考えます。
- 国からの資金援助が全く受けられず、共同研究者である東京大学医科学研究所(当時)の中村祐輔教授(シカゴ大学医学部教授を経て現在がんプレシジョン医療研究センター所長)の大変な尽力で立ち上げたワクチン開発を期待する患者支援団体である"Captivation Network"からの寄付で全ての臨床試験と附随する研究が行われたという点です。つまり、病気に苦しみつつも新薬を期待する患者さんの善意と希望による支援でなし得た研究です。この場を借りてご支援を頂きました患者の皆様に心より御礼申し上げると共に、ペプチドワクチンの保険承認ということで皆様のお気持ちにお応えしていくことができればと願う次第です。